IKATAN KIMIA DAN UNSUR KIMIA
IKATAN
KIMIA DAN UNSUR KIMIA
A. IKATAN
KIMIA
Ikatan
kimia adalah sebuah proses fisika yang bertanggung jawab dalam
interaksi gaya tarik menarik antara dua atom atau molekul yang menyebabkan suatu
senyawa diatomik atau poliatomik menjadi
stabil. Penjelasan mengenai gaya tarik menarik ini sangatlah rumit dan
dijelaskan oleh elektrodinamika
kuantum. Dalam praktiknya, para kimiawan biasanya bergantung
pada teori kuantum atau
penjelasan kualitatif yang kurang kaku (namun lebih mudah untuk dijelaskan)
dalam menjelaskan ikatan kimia. Secara umum, ikatan kimia yang kuat
diasosiasikan dengan transfer elektron antara dua atom yang berpartisipasi.
Ikatan kimia menjaga molekul-molekul, kristal, dan gas-gas diatomik untuk tetap
bersama. Selain itu ikatan kimia juga menentukan struktur suatu zat.
Kekuatan ikatan-ikatan kimia sangatlah bervariasi. Pada umumnya, ikatan kovalen dan ikatan ion dianggap sebagai ikatan
"kuat", sedangkan ikatan hidrogen dan ikatan van der Waals dianggap
sebagai ikatan "lemah". Hal yang perlu diperhatikan adalah bahwa
ikatan "lemah" yang paling kuat dapat lebih kuat daripada ikatan
"kuat" yang paling lemah.
1.
IKATAN KUAT KIMIA
Bentuk atom-atom dan molekul-molekul yang 3 dimensi
sangatlah menyulitkan dalam menggunakan teknik tunggal yang mengindikasikan
orbital-orbital dan ikatan-ikatan. Pada rumus molekul, ikatan kimia (orbital yang berikatan) diindikasikan
menggunakan beberapa metode yang bebeda tergantung pada tipe diskusi.
Kadang-kadang kesemuaannya dihiraukan. Sebagai contoh, pada kimia organik, kimiawan biasanya hanya peduli pada gugus
fungsi molekul. Oleh karena itu, rumus molekul etanol dapat
ditulis secara konformasi, 3-dimensi, 2-dimensi penuh (tanpa indikasi arah ikatan
3-dimensi), 2-dimensi yang disingkat (CH3–CH2–OH), memisahkan gugus fungsi dari bagian molekul lainnnya (C2H5OH), atau hanya dengan konstituen atomnya saja (C2H6O). Kadangkala, bahkan kelopak valensi elektron non-ikatan
(dengan pendekatan arah yang digambarkan secara 2-dimensi) juga ditandai.
Beberapa kimiawan juga menandai orbital-orbital atom, sebagai contoh anion etena−4 yang
dihipotesiskan (\/C=C/\ −4) mengindikasikan kemungkinan pembentukan ikatan.sehingga
terjadi ikatan rangkap dua. Berikut beberapa ikatan kuat kimia:
a.
Ikatan ionik
Ikatan ionik (ikatan elektrovalen):
“transfer elektron”Atom logam (energi ionisasi rendah) cenderung melepaskan
elektronnya, lalu diterima oleh atom nonlogam (afinitas elektron besar). Dari
proses transfer elektron dari atom logam ke atom nonlogam ini akan terbentuk
ion positif dan ion negatif dengan konfigurasi elektron gas mulia
yang saling tarik menarik dengan gaya elektrostatis yang disebut ikatan ionik.
Sebagai contoh, dalam pembentukan senyawa ionik NaCl terjadi transfer elektron
dari atom Na ke atom Cl 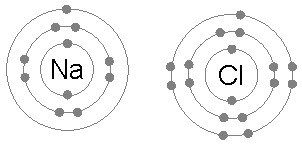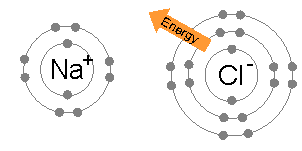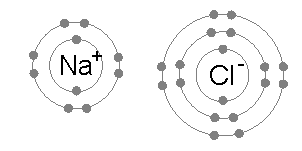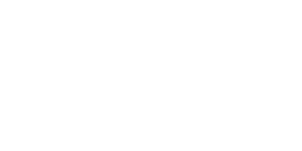

Di dalam senyawa, ion positif dan
negatif tersusun dalam jumlah tertentu. Sebagai contoh senyawa NaCl yang
berbentuk kristal sebenarnya membentuk struktur kubus. Tiap-tiap ion Na+ dikelilingi oleh ion Cl– sejumlah 6 ion. Beberapa
sifat senyawa ion yaitu membentuk kristal namun rapuh, titik lebur dan titik
lelehnya tinggi, mudah sekali larut dalam air, dan mampu menghantarkan arus
listrik.
b.
Ikatan logam
Ikatan logam adalah
ikatan kimia yang memiliki ciri-ciri yaitu bisa menjadi penghantar panas maupun
arus listrik, dapat atau mudah ditempa, bersifat ulet, dan juga bisa diulur
menjadi kawat. Pembentukan ikatan ion terjadi karena adanya perbedaan energi
ionisasi dan afinitas elektron suatu atom. Ikatan
logam terdiri dari ion logam yang positif di lautan elektron yang merupakan
valensi elektron dari setiap atom dan saling bertumpang tindih.
Elektron-elektron tersebut bebas bergerak dan mengelilingi inti di dalam
kristal. Elektron yang bisa bebas bergerak ini dikenal dengan sebutan elektron
dislokasi. Sedangkan gaya tarik antar atom-atom menyebabkan terjadinya ikatan
logam. Karena elektron-elektron di dalam logam dapat bebas bergerak maka logam
dapat menghantarkan panas atau kalor dan arus listrik. Sehingga logam banyak
dimanfaatkan dalam alat-alat listrik dan rumah tangga.

c. Ikatan Kovalen
Ikatan kovalen
adalah ikatan yang terjadi karena adanya pemakaian pasangan elektron secara
bersama-sama. Namun jika pasangan elektron yang dipakai bersama itu berasal
dari salah satu atom, ikatan ini disebut sebagai ikatan kovalen koordinasi. Sebagai
contoh yaitu pada molekul hidrogen. Dalam molekul hidrogen terdapat dua atom
hidrogen yang saling berikatan membentuk ikatan kovalen. Masing-masing atom
hidrogen menyumbangkan 1 elektronnya sehingga membentuk pasangan elektron yang
berikatan dan digunakan bersama-sama. Ada berbagai senyawa yang merupakan
ikatan kovalen misalnya O2, NH3, SO3, dan sebagainya.
Di dalam senyawa kovalen juga ada bisa membentuk ikatan tunggal yang disebut
sebagai ikatan kovalen tunggal. Lalu ada senyawa dengan ikatan rangkap dua yang
disebut dengan ikatan kovalen rangkap dua. Selain itu terdapat juga ikatan
kovalen rangkap tiga. Dalam ikatan kovalen juga bisa terjadi penyimpangan
kaidah oktet. Penyimpangan ini bisa terjadi pada senyawa BF3, CO, dan PCl5. Di dalam
senyawa tersebut susunan elektron tidak duplet maupun oktet. Sehinggal memiliki
struktur yang berbeda dari senyawa yang lain.
d. Ikatan 3c-2e dan 3c-4e
Dalam ikatan tiga-pusat dua-elektron,
tiga atom saling berbagi dua elektron. Ikatan sejenis ini terjadi pada senyawa
yang kekurangan elektron seperti pada diborana.
Setiap ikatan mengandung sepasang elektron yang menghubungkan atom boron satu
sama lainnya dalam bentuk pisang dengan sebuah proton (inti atom hidrogen) di
tengah-tengah ikatan, dan berbagi elektron dengan kedua atom boron. Terdapat
pula Ikatan tiga-pusat empat-elektron yang
menjelaskan ikatan pada molekul hipervalen.
e.
Kepolaran Ikatan, Elektronegativitas, dan Momen Dipol
Ikatan kimia di mana
elektron-elektron digunakan bersama secara setara dan merata, seperti pada Cl2 dan N2, disebut sebagai
ikatan kovalen nonpolar. Ikatan di mana salah satu atom memiliki daya tarik
elektron (elektronegativitas) yang lebih tinggi terhadap elektron-elektron
ikatan dibanding atom lainnya, sehingga terjadi pembentukan dipol (pemisahan
muatan negatif dan muatan positif), seperti pada HF, disebut sebagai ikatan
kovalen polar.
Ukuran kepolaran dinyatakan dengan besaran yang
disebut momen dipol (μ). Semakin besar momen dipol, semakin besar kepolarannya.
Satuan momen dipol adalah debye (D), di mana 1 D = 3,34×10−30 Cm. Jika dua muatan
berlawanan dengan besar muatan sama Q+ dan Q− terpisah dengan jarak r, maka
momen dipolnya adalah hasil kali Q dan r: μ = Qr
B.
KIMIA UNSUR
Kimia unsur menjadi ilmu kimia yang mempelajari secara
spesifik mengenai atom dan klasifikasinya berdasarkan sifat. Segala sesuatu
yang berada di alam semesta ini semuanya tersusun oleh atom yang saling
bergabung membentuk molekul. Setiap atom itu memiliki karakteristik dan sifat
yang berbeda sehingga dapat dikelompokkan menjadi sub kelompok.
Konsep
teori kimia modern yang ada saat ini merupakan hasil yang berasal dari sejarah
masa lalu. Teori tentang atom dan unsur telah banyak berubah dan banyak gagasan
yang muncul untuk teori ini.
Ahli
kimia asal Perancis yaitu Antoine Laurent Lavoisier menjadi salah satu yang
paling berpengaruh dimana dia mengembangkan hasil teori Robert Boyle dari
Inggris yang menekankan tentang sifat fisik suatu unsur dan menghubungkannya
dengan senyawa yang dapat dibentuk dengan sifat itu. Lavoisier berhasil mengklasifikasikan unsur berdasarkan definisi
dari Boyle dimana daftar unsur yang dibuat oleh Lavoisier ini didasarkan pada
penelitian.
1.
PENGERTIAN
UNSUR
Unsur kimia merupakan suatu zat yang tidak bisa
diuraikan lagi menjadi zat yang lebih sederhana dengan proses kimia biasa,
dengan kata lain unsur adalah bahan dasar atau terkecil yang menyusun semua
materi.
Setiap unsur unik atau memiliki sifat karakteristiknya
sendiri yang berbeda untuk setiap unsur lain. Biasanya untuk memudahkan, setiap
unsur diwakili dengan simbol berupa huruf. Seperti H untuk hidrogen, O untuk
oksigen atau C untuk karbon. Selain itu, setiap elemen memiliki nomor atom dan
berat atom yang berbeda. Unsur juga dikenal dengan sebutan atom.
Saat ini terdapat 118 unsur kimia yang dikenal dengan
20% diantaranya tidak tersedia di alam dan hanya diketahui melalui sintesis
laboratorium. Setiap unsur dapat bergabung satu sama lain untuk membentuk
berbagai macam zat yang lebih kompleks atau disebut senyawa.
Jumlah senyawa yang mungkin terbentuk dari unsur
sangatlah tidak terbatas. Ketika dua atau lebih unsur membentuk senyawa, maka
mereka akan kehilangan sifat dan identitas awal mereka sebagai suatu unsur dan
memiliki sifat dan identitas baru sebagai senyawa.
2.
ATOM
Karakteristik dari kimia unsur sangat terkait erat
dengan jumlah dan pengaturan elektron yang ada di dalam atom. Dengan demikian,
unsur-unsur kimia yang ada saat ini dapat dibedakan satu sama lain oleh nomor
atomnya. Berdasarkan hal tersebut, maka para ahli kimia telah menemukan
klasifikasi unsur kimia yang akan memudahkan kita melalui yang dikenal dengan
tabel periodik unsur.
3. TABEL PERIODIK UNSUR
Tabel periodik adalah suatu tabel yang mengatur
semua unsur kimia yang dikenal dalam suatu bentuk yang informatif. Unsur-unsur
kimia disusun dari kiri ke kanan dan dari atas ke bawah dalam urutan
peningkatan nomor atom. Kenaikan nomor atom tersebut juga diikuti dengan
kenaikan massa dari atom itu sendiri.
Dalam tabel periodik, baris disebut dengan periode.
Tingkat periode suatu unsur kimia menunjukkan tingkat energi tertinggi yang
dimiliki oleh elektron dalam unsur tersebut dalam keadaan dasar. Dalam satu
baris atau dalam satu periode, tingkat energi atom meningkat dari kiri ke
kanan.
Sedangkan unsur yang menempati kolom disebut dengan
golongan. Atom yang berada dalam satu golongan cenderung memiliki konfigurasi
elektron yang identik dan akibatnya memiliki perilaku yang sama secara kimiawi.
Berikut ini merupakan contoh dari tabel periodik unsur:

Bermanfaat. Terimakasih
BalasHapusSangat bermanfaat kak, mkasih
BalasHapusBagus bang
BalasHapusbagus dan membantu
BalasHapusNice blognya
BalasHapusThanks sangat membantu dan bermanfaat
BalasHapus